| OBJETIVO
:
Comprobar que el agua hierve a una temperatura menor de su punto de ebullición cuando la presión atmosférica es menor de una atmósfera. |
MATERIAL :
- 1 jeringa - agua a temperatura ambiente.
|
Tapa con tu dedo el orificio de salida del líquido y sin dejar de hacerlo jala el émbolo de la jeringa hacia afuera. |
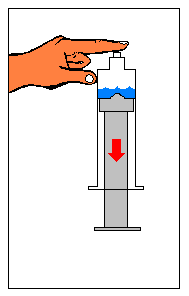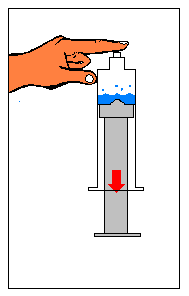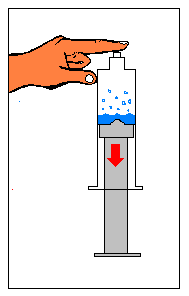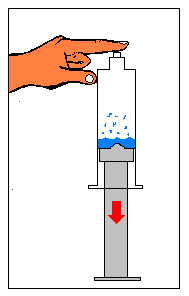 |
1.- ¿ Qué sucede con
el agua dentro de la jeringa ?
R=
2.-¿ Qué sucede si repentinamente destapas el orificio
?
R=
|
|
Da los siguientes valores: masa de 0.1 Kg, temperatura inicial de 0ºC, temperatura final no le asignes valor, presión asignale un valor menor de "1.0" y oprime el botón de "Empezar". La presión la vas variando hasta encontrar el valor con el cual la El valor de la PRESIÓN fue de:_______ |

|